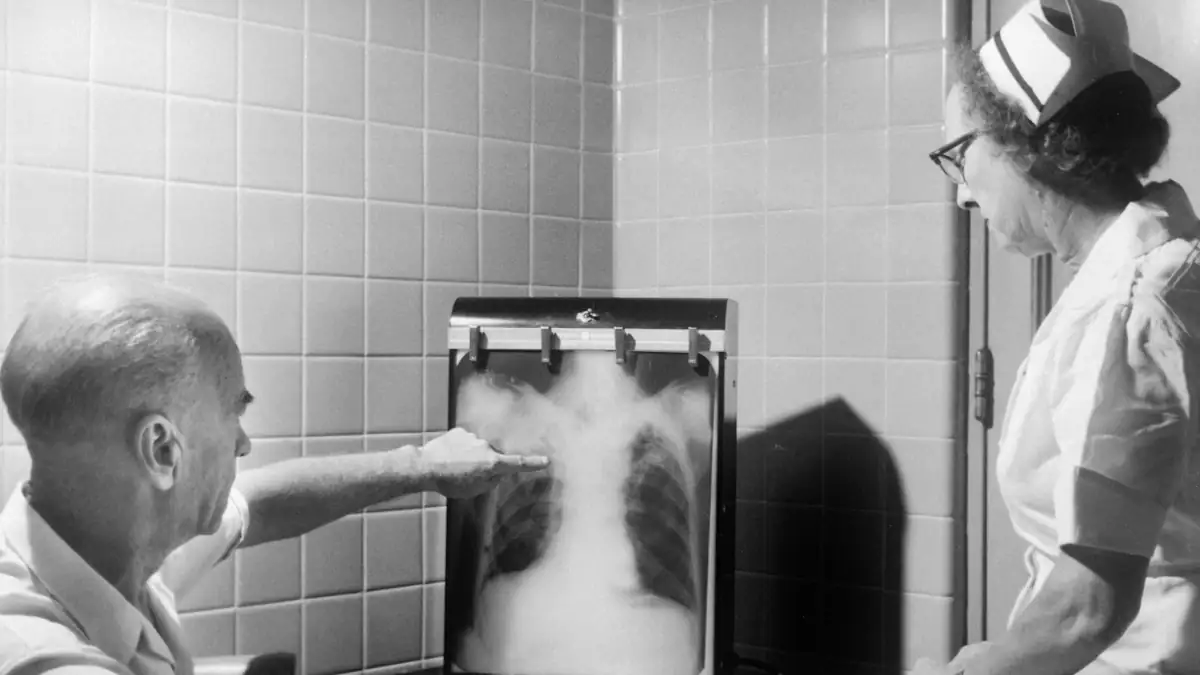
Le cancer du poumon reste la première cause de mortalité par cancer dans le monde, avec 2,48 millions de nouveaux cas et 1,8 million de décès recensés en 2022, selon les données GLOBOCAN de l’Agence internationale de recherche sur le cancer (AIRC). Si le tabac en est responsable dans environ 85 % des cas à l’échelle mondiale, une part croissante des malades n’a jamais fumé — et les facteurs en cause restent largement sous-estimés.
La toux persistante ou modifiée constitue le premier signal clinique à prendre au sérieux. Elle peut s’accompagner de crachats teintés de sang, d’un essoufflement inhabituel ou d’une fatigue inexpliquée. Chez les patients déjà atteints de bronchite chronique, c’est la modification de leur toux habituelle qui doit alerter. Le problème : la maladie est le plus souvent asymptomatique à ses stades précoces, ce qui explique la fréquence des diagnostics tardifs.
Le radon et l’amiante, deux dangers professionnels et domestiques
Le radon, gaz radioactif naturellement présent dans les sols granitiques et volcaniques, est la deuxième cause de cancer du poumon après le tabac. L’Organisation mondiale de la santé (OMS) estime qu’il est à l’origine de 3 à 14 % des cas selon les pays, avec un risque qui augmente d’environ 16 % pour chaque hausse de 100 becquerels par mètre cube dans l’air intérieur. L’amiante, quant à elle, multiplie par cinq le risque de cancer pulmonaire selon la Fondation ARC pour la recherche sur le cancer. Combinée au tabac, cette exposition peut porter le risque à 50 à 90 fois celui de la population générale. L’Institut national de recherche et de sécurité (INRS) estime qu’environ 15 % des cancers du poumon sont d’origine professionnelle.
Pollution atmosphérique et domestique : des risques confirmés à l’échelle moléculaire
L’Agence européenne pour l’environnement attribue à la pollution atmosphérique environ 9 % des cancers du poumon en Europe. Une étude internationale publiée dans Nature en juillet 2025, menée sur 871 patients répartis sur quatre continents dans le cadre du projet Sherlock-Lung, a établi que les non-fumeurs exposés à de fortes concentrations de particules fines présentaient presque quatre fois plus de mutations génétiques associées habituellement au tabagisme. Le mécanisme identifié est une inflammation chronique qui transforme des cellules déjà mutées en tumeurs.
À l’intérieur des foyers, d’autres sources de pollution sont également pointées. La combustion du bois, du charbon et les fumées de cuisson à haute température dans des espaces mal ventilés constituent un facteur de risque reconnu, notamment chez les femmes en Asie. Les bougies à base de paraffine, dérivée du pétrole, libèrent lors de la combustion des composés organiques volatils dont le benzène et le formaldéhyde — deux substances classées cancérigènes par l’AIRC. Des particules de suie ultrafines, comparables aux émissions diesel par leur taille et leur composition, pénètrent profondément dans les voies respiratoires. La Dre Sarah Evans, de l’École de médecine Icahn du Mont Sinaï, indique que « les bougies allumées contribuent à une mauvaise qualité de l’air et augmentent le risque d’exposition par inhalation à des produits chimiques préoccupants ». Le risque reste toutefois conditionné à la fréquence d’usage et à la ventilation des espaces.
Une composante génétique héréditaire désormais documentée
La prédisposition génétique constitue le cinquième facteur identifié. Selon des études menées sur des jumeaux, l’héritabilité du cancer du poumon est estimée à 18 %, proportion comparable à celle du cancer du côlon. Deux gènes majeurs sont impliqués : TP53 et EGFR, tous deux associés aux adénocarcinomes pulmonaires. Ces formes génétiques surviennent généralement avant 50 ans, souvent chez des non-fumeurs. Des mutations dans les gènes BRCA1, BRCA2, CHEK2 et ATM ont également été identifiées dans des familles à antécédents multiples, selon la Société de Pneumologie de Langue Française.
Si les projections de GLOBOCAN anticipent 4,62 millions de nouveaux cas mondiaux d’ici 2050 en l’absence de changement des tendances actuelles, des programmes de dépistage par scanner faible dose sont déjà recommandés pour les populations à risque génétique identifié, avec un suivi préconisé dès l’âge de 20 à 25 ans pour les porteurs de mutations constitutionnelles d’EGFR.